Termodinamika – Pengertian, Konsep, Proses, Rumus dan Contohnya – Termodinamika (bahasa Yunani: thermos = ‘panas’ and dynamic = ‘perubahan’) adalah fisika energi, panas, kerja, entropi dan kespontanan proses. Termodinamika berhubungan dekat dengan mekanika statistik di mana banyak hubungan termodinamika berasal. Pada sistem di mana terjadi proses perubahan wujud atau pertukaran energi, termodinamika klasik tidak berhubungan dengan kinetika reaksi (kecepatan suatu proses reaksi berlangsung). Karena alasan ini, penggunaan istilah “termodinamika” biasanya merujuk pada termodinamika setimbang. Dengan hubungan ini, konsep utama dalam termodinamika adalah proses kuasistatik, yang diidealkan, proses “super pelan”. Proses termodinamika bergantung-waktu dipelajari dalam termodinamika tak-setimbang.

Karena termodinamika tidak berhubungan dengan konsep waktu, telah diusulkan bahwa termodinamika setimbang seharusnya dinamakan termostatik. Hukum termodinamika kebenarannya sangat umum, dan hukum-hukum ini tidak bergantung kepada rincian dari interaksi atau sistem yang diteliti. Ini berarti mereka dapat diterapkan ke sistem di mana seseorang tidak tahu apa pun kecual perimbangan transfer energi dan wujud di antara mereka dan lingkungan. Contohnya termasuk perkiraan Einstein tentang emisi spontan dalam abad ke-20 dan riset sekarang ini tentang termodinamika benda hitam.
Simak Juga : Gas Ideal dan Teori Kinetik Gas – Pengertian, Rumus, dan Contohnya
A. Pengertian Termodinamika
Termodinamika adalah kajian tentang kalor (panas) yang berpindah. Dalam termodinamika kamu akan banyak membahas tentang sistem dan lingkungan. Kumpulan benda-benda yang sedang ditinjau disebut sistem, sedangkan semua yang berada di sekeliling (di luar) sistem disebut lingkungan.
Termodinamika secara sederhana dapat diartikan sebagai ilmu pengetahuan yang membahas dinamika panas suatu sistem. Termodinamika merupakan sains eksperimental yang berdasar pada sejumlah kecil prinsip yang digeneralisasi dari pengalaman atau pengamatan. Dari prinsip-prinsip ini diturunkan hubungan umum antara aneka kuantitas makroskopik yang dipengaruhi oleh perubahan panas seperti kapasitas kalor jenis, koefisien magnetik dan dieletrik suatu bahan (Atkins, PW. 1994. Kimia Fisik II. Erlangga: Jakarta).
Ada beberapa pengertian dari Termodinamika:
- Termodinamika adalah cabang ilmu fisika yang mempelajari pertukaran energi dalam bentuk kalor dan kerja, sistem pembatas (boundary) serta lingkungan.
- Termodinamika adalah ilmu yang mempelajari hubungan antara panas, kerja mekanik serta aspek-aspek lain dari energi dan perpindahannya.
- Termodinamika adalah suatu cabang ilmu fisika yang mempelajari hukum-hukum dasar yang dipatuhi oleh kalor dan usaha.
B. Sistem Termodinamika
Sistem termodinamika adalah bagian dari jagat raya yang diperhitungkan. Sebuah batasan yang nyata atau imajinasi memisahkan sistem dengan jagat raya, yang disebut lingkungan. Klasifikasi sistem termodinamika berdasarkan pada sifat batas sistem-lingkungan dan perpindahan materi, kalor dan entropi antara sistem dan lingkungan.
Sistem dalam termodinamika merujuk pada bagian tertentu dari semesta (universe) di dalam permukaan tertutup yang disebut batas atau dinding dari sistem. Suatu sistem dapat mengalami pertukaran energi dengan sistem lain atau bagian luar diding yang disebut lingkungan dari sistem yang bersangkutan. Sistem bersama lingkungannya membentuk semesta.
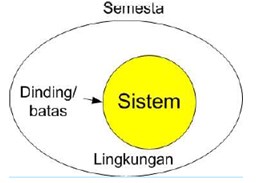
Ada tiga jenis sistem berdasarkan jenis pertukaran yang terjadi antara sistem dan lingkungan:
Sistem Terisolasi
tak terjadi pertukaran panas, benda atau kerja dengan lingkungan. Contoh dari sistem terisolasi adalah wadah terisolasi, seperti tabung gas terisolasi.
Sistem Tertutup
terjadi pertukaran energi (panas dan kerja) tetapi tidak terjadi pertukaran benda dengan lingkungan. Rumah hijau adalah contoh dari sistem tertutup di mana terjadi pertukaran panas tetapi tidak terjadi pertukaran kerja dengan lingkungan. Apakah suatu sistem terjadi pertukaran panas, kerja atau keduanya biasanya dipertimbangkan sebagai sifat pembatasnya:
- pembatas adiabatik: tidak memperbolehkan pertukaran panas.
- pembatas rigid: tidak memperbolehkan pertukaran kerja.
Sistem Terbuka
terjadi pertukaran energi (panas dan kerja) dan benda dengan lingkungannya. Sebuah pembatas memperbolehkan pertukaran benda disebut permeabel. Samudra merupakan contoh dari sistem terbuka.
Dalam kenyataan, sebuah sistem tidak dapat terisolasi sepenuhnya dari lingkungan, karena pasti ada terjadi sedikit pencampuran, meskipun hanya penerimaan sedikit penarikan gravitasi. Dalam analisis sistem terisolasi, energi yang masuk ke sistem sama dengan energi yang keluar dari system (Chang, R. 1995. Chemistry. Random House: USA).
C. Hukum Pertama Termodinamika
Hukum Pertama Termodinamika (kekekalan energi)
Menyatakan perubahan energi dalam dari suatu sistem termodinamika tertutup sama dengan total dari jumlah energi kalor yang disuplai ke dalam sistem dan kerja yang dilakukan terhadap sistem.
“Perubahan energi dalam (U) sistem pada suatu prosessama dengan aliran panas total (Q) ke dalam sistem dikurangi kerja (W) yang dilakukan sistem”( Sukardjo. 1989. Kimia Anorganik. Bina Aksara: Yogyakarta).
U2 – U1 = Q – W ~ kekekalan energi
Hukum 1 Termodinamika
Hukum ini berbunyi: “Kalor dan kerja mekanik adalah bisa saling tukar”. Sesuai dengan hukum ini, maka sejumlah kerja mekanik dibutuhkan untuk menghasilkan sejumlah kalor, dan sebaliknya. Hukum ini bisa juga dinyatakan sebagai: “Energi tidak bisa dibuat atau dimusnahkan, namun bisa dirubah dari satu bentuk kebentuk lainnya”. Sesuai dengan hukum ini, energi yang diberikan oleh kalor mesti sama dengan kerja eksternal yang dilakukan ditambah dengan perolehan energy dalam karena kenaikan temperatur.
Jika kalor diberikan kepada sistem, volume dan suhu system akan bertambah (system akan terlihat mengembang dan bertambah panas). Sebaliknya, jika kalor diambil dari sistem, volume dan suhu system akan berkurang (system tampak mengerut dan terasa lebih dingin). Prinsip ini merupakan hukum alam yang penting dan salah satu bentuk dari hukum kekekalan energi.
Sistem yang mengalami perubahan volume akan melakukan usaha dan sistem yang mengalami perubahan suhu akan mengalami perubahan energy dalam. Jadi, kalor yang diberikan kepada system akan menyebabkan system melakukan usaha dan mengalami perubahan energy dalam.
Prinsip ini dikenal sebagai hukum kekekalan energy dalam termodinamika atau disebut Hukum I Termodinamika.Untuk suatu proses dengan keadaan akhir (2) dan keadaan awal (1)
∆U = U2–U1
Temodinamika merupakan cabang ilmu fisika yang mempelajari mengenai pengaliran panas, perubahan-perubahan energi yang diakibatkan dan usaha yang dilakukan oleh panas.
Usaha luar ( W )
yaitu : Usaha yang dilakukan oleh system terhadap sekelilingnya terhadap sistem. Misalkan gas dalam ruangan yang berpenghisap bebas tanpa gesekan dipanaskan ( pada tekanan tetap ) ; maka volume akanbertambahdengan V.
Usaha yang dilakukanoleh gas terhadap udara luar :
W = p.V
Usaha dalam ( U )
adalah : Usaha yang dilakukan oleh bagian dari suatu system pada bagian lain dari system itu pula. Pada pemanasan gas seperti di atas, usaha dalam adalah berupa gerakan-gerakan antara molekul-molekul gas yang dipanaskan menjadi lebih cepat.
Secara matematis, Hukum I Termodinamika dituliskan sebagai
Q = W + ∆U
Dimana
Q = kalor yang masuk/keluarsistem
U = perubahanenergidalam
W = Usaha luar.
Q positif, sistem menerima kalor.
Q negatif, sistem melepas kalor.
W positif, sistem melakukan usaha.
W negatif, sistem menerima usaha.
positif, terjadi penambahan energi dalam pada sistem.
negatif, terjadi penurunan energi dalam pada sistem.

Kalor (Q)
merupakan energi yang berpindah dari satu benda ke benda yang lain akibat adanya perbedaan suhu. Berkaitan dengan sistem dan lingkungan, bisa dikatakan bahwa kalor merupakan energi yang berpindah dari sistem ke lingkungan atau energi yang berpindah dari lingkungan ke sistem akibat adanya perbedaan suhu. Jika suhu sistem lebih tinggi dari suhu lingkungan, maka kalor akan mengalir dari sistem menuju lingkungan. Sebaliknya, jika suhu lingkungan lebih tinggi dari suhu sistem, maka kalor akan mengalir dari lingkungan menuju sistem.
Jika Kalor (Q) berkaitan dengan perpindahan energi akibat adanya perbedaan suhu, maka Kerja (W) berkaitan dengan perpindahan energi yang terjadi melalui cara-cara mekanis. Misalnya jika sistem melakukan kerja terhadap lingkungan, maka energi dengan sendirinya akan berpindah dari sistem menuju lingkungan. Sebaliknya jika lingkungan melakukan kerja terhadap sistem, maka energi akan berpindah dari lingkungan menuju sistem.
Baca Juga : Suhu dan Kalor – Pengertian, Rumus, Hubungan dan Contohnya
D. Proses-proses dalam Termodinamika
Proses Isotermik
Suatu sistem dapat mengalami proses termodinamika dimana terjadi perubahan-perubahan di dalam sistem tersebut. Jika proses yang terjadi berlangsung dalam suhu konstan, proses ini dinamakan proses isotermik. Karena berlangsung dalam suhu konstan, tidak terjadi perubahan energi dalam (∆U = 0) dan berdasarkan hukum I termodinamika kalor yang diberikan sama dengan usaha yang dilakukan sistem (Q = W).
Proses Isokhorik
Jika gas melakukan proses termodinamika dalam volume yang konstan, gas dikatakan melakukan proses isokhorik. Karena gas berada dalam volume konstan (∆V = 0), gas tidak melakukan usaha (W = 0) dan kalor yang diberikan sama dengan perubahan energi dalamnya. Kalor di sini dapat dinyatakan sebagai kalor gas pada volume konstan QV.
QV = ∆U
Proses Isobarik
Jika gas melakukan proses termodinamika dengan menjaga tekanan tetap konstan, gas dikatakan melakukan proses isobarik. Karena gas berada dalam tekanan konstan, gas melakukan usaha (W = p∆V). Kalor di sini dapat dinyatakan sebagai kalor gas pada tekanan konstan Qp. Berdasarkan hukum I termodinamika, pada proses isobarik berlaku :
Sebelumnya telah dituliskan bahwa perubahan energi dalam sama dengan kalor yang diserap gas pada volume konstan
QV =∆U
Dari sini usaha gas dapat dinyatakan sebagai
W = Qp − QV
Jadi, usaha yang dilakukan oleh gas (W) dapat dinyatakan sebagai selisih energi (kalor) yang diserap gas pada tekanan konstan (Qp) dengan energi (kalor) yang diserap gas pada volume konstan (QV).
Proses Adiabatik
Dalam proses adiabatik tidak ada kalor yang masuk (diserap) ataupun keluar (dilepaskan) oleh sistem (Q = 0). Dengan demikian, usaha yang dilakukan gas sama dengan perubahan energi dalamnya (W = ∆U).
Jika suatu sistem berisi gas yang mula-mula mempunyai tekanan dan volume masing-masing p1 dan V1 mengalami proses adiabatik sehingga tekanan dan volume gas berubah menjadi p2 dan V2.
Dimana γ adalah konstanta yang diperoleh perbandingan kapasitas kalor molar gas pada tekanan dan volume konstan dan mempunyai nilai yang lebih besar dari 1 (γ > 1).
E. Sifat-sifat Termodinamika
Adapun sifat-sifat dalam termodinamika sebagai berikut:
Variabel/fungsi keadaan
— Nilai yang ditentukan dari kondisi sekarang dan tidak tergantung dari lintasan (T, p, V, komposisi).
Variabel proses
— Hanya memiliki arti untuk sistem yang berubah.
Sifat intensif
— Memiliki nilai pada setiap kedudukan di dalam sistem. Tidak tergantung pada kuantitas materi
Contoh: Temperatur, tekanan, massa jenis, titik didih, pH, Tegangan muka, Indeks bias, kekentalan, panas spesifik
Sifat Ekstensif
— Merupakan nilai untuk keseluruhan sistem. Tergantung dari kuantitas materi
Contoh: massa, Volume, Energi Dalam, Entalpi, entropi
Sudah selesai membaca materi ini ? Ayo lihat dulu Daftar Materi Fisika



