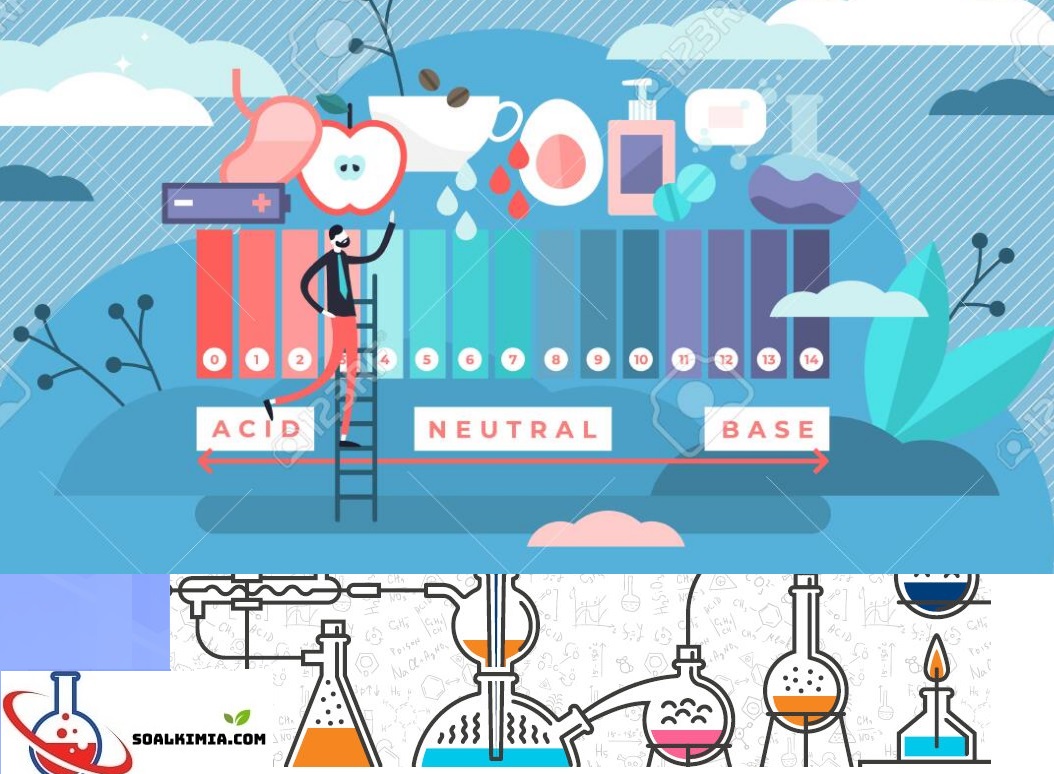
Derajat Keasaman (pH)
Konsentrasi ion hidronium [H+] dalam suatu larutan encer relatif kecil tetapi sangat menentukan sifat-sifat larutan, terutama larutan dalam air. Sorensen (1868 – 1939) mengusulkan konsep “pH” (pangkat ion hidrogen) agar memudahkan pengukuran dan perhitungan untuk mengikuti perubahan konsentrasi ion H+ dalam suatu larutan. Menurut sorensen, pH merupakan fungsi negatif logaritma dari konsentrasi ion H+ dalam suatu larutan, dan dirumuskan sebagai berikut.
pH = – log [H+]
Dengan analogi yang sama, untuk menentukan nilai konsentrasi OH– dalam larutan dapat digunakan rumus nilai pOH.
pOH = – log [OH–]
Dalam kesetimbangan air terdapat tetapan kesetimbangan :
Kw = [H+] [OH–]
Contoh
Hitunglah pH air murni pada suhu 25°
jawab :
pH = -log 10-7
= -(-7)
= 7
Oleh karena [H+] dan [OH–] dalam air murni adalah sama, dapat ditentukan pula nilai pOH pada air murni.
pOH = -log [OH–]
= -log 10-7
= 7
atau dengan menggunakan rumus :
pH + pOH = 14
7 + pOH = 14
pOH = 7
1. Nilai pH dan Sifat Larutan
Air murni mempunyai nilai pH = 7 dan pOH = 7. Bagaimana nilai pH larutan yang bersifat asam atau bersifat basa ? Beberapa contoh berikut dapat digunakan untuk menemukan hubungan nilai pH dan pOH dengan kondisi suatu larutan.
Larutan asam kuat HCl 0,1 M
jawab :
HCl(aq) → H+(aq) + Cl–(aq)
0,1 M 0,1 M
[H+] = 0,1 M
pH = -log 0,1
pH = 1
Oleh karena larutan dalam air, nilai pOH dapat ditentukan berdasarkan nilai tetapan kesetimbangan air Kw = 10-14
[H+] [OH–] = 10-14
0,1 [OH–] = 10-14
[OH–] = 10-13 M
pOH = -log 10-13
pOH = 13
Larutan asam lemah CH3COOH 0,1 M Ka = 10-5
jawab :
[H+] = 10-3
pH = -log 10-3
pH = 3
pOH = 14 – pH
pOH = 11
Larutan basa kuat NaOH 0,1 M
NaOH(aq) → Na+(aq) + OH–(aq)
jawab :
0,1 M 0,1 M
[OH–] = 0,1 M
pOH = -log 0,1
pOH = 1
pH + pOH = 14
pH + 1 = 14
pH = 13
Basa lemah NH4OH 0,1 M, Kb = 10-5
jawab :
[OH–] = 10-3
pOH = pOH -log 10-3
pOH = 3
pH = 14 – pOH
pH = 11
Nilai pH dapat memberikan informasi tentang kekuatan suatu asam atau basa. Untuk konsentrasi yang sama, semakin kuat suatu asam, semakin besar konsentrasi ion H+ dalam larutan, dan nilai pH-nya semakin kecil. Semakin kuat suatu asam, semakin kecil nilai pH-nya. Sebaliknya semakin kuat suatu basa, semakin besar konsentrasi ion OH– dalam larutan. Semakin besar konsentrasi ion OH–, semakin kecil konsentrasi ion H+ dalam larutan. Akibatnya, nilai pH menjadi semakin besar. Semakin kuat suatu basa, semakin besar nilai pH-nya.
2. Indikator Asam Basa dan Nilai pH
Untuk mengetahui nilai pH suatu larutan dapat dilakukan dengan menggunakan pH meter atau indikator universal.

pH meter merupakan suatu rangkaian alat elektronik yang dilengkapi dengan elektroda kaca. Jika elektroda kaca ini dimasukan kedalam larutan, akan timbul beda potensial yang diakibatkan oleh adanya ion H+ dalam larutan. Besarnya beda potensial ini ditunjukan dengan angka yang menyatakan pH larutan tersebut.
Indikator universal adalah indikator pH berisi larutan dari beberapa senyawa yang menunjukkan beberapa perubahan warna yang halus pada rentang pH antara 1-14 untuk menunjukkan keasaman atau kebasaan larutan.
Selain itu asam basa dapat ditentukan dengan indikator asam basa yang merupakan suatu zat yang mempunyai warna tertentu pada pH tertentu. Sebagai contoh bromtimol biru (BTB) akan berwarna kuning dalam lingkungan asam, berwarna biru dalam basa, dan berwarna hijau pada suasana netral.
Indikator tunggal hanya akan menunjuk hasil secara umum, misalnya suatu larutan ditetesi indikator PP berwarna merah, berarti larutan tersebut mempunyai pH > 8,3. Untuk mendapatkan hasil yang lebih teliti dapat digunakan beberapa indikator terhadap satu larutan,
Sudah selesai membaca materi ini ? Ayo lihat dulu Daftar Materi Kimia