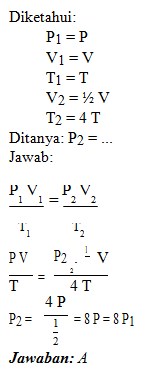Contoh Soal Teori Kinetik Gas Pilihan Ganda dan Jawaban – Teori Kinetik (atau teori kinetik pada gas) berupaya menjelaskan sifat-sifat makroscopik gas, seperti tekanan, suhu, atau volume, dengan memperhatikan komposisi molekular mereka dan gerakannya.
Intinya, teori ini menyatakan bahwa tekanan tidaklah disebabkan oleh denyut-denyut statis di antara molekul-molekul, seperti yang diduga Isaac Newton, melainkan disebabkan oleh tumbukan antarmolekul yang bergerak pada kecepatan yang berbeda-beda.
Teori Kinetik dikenal pula sebagai Teori Kinetik-Molekular atau Teori Tumbukan atau Teori Kinetik pada Gas.
1 – 10 Contoh Soal Teori Kinetik Gas dan Jawaban
1. Gas ideal berada dalam ruang tertutup dengan volume V, tekanan P dan suhu T. Apabila volumenya mengalami perubahan menjadi 1/2 kali semula dan suhunya dinaikkan menjadi 4 kali semula, maka tekanan gas yang berada dalam sistem tersebut menjadi….
A. 8 P1
B. 2 P1
C. 1/2 P1
D. 1/4 P1
E. 1/8 P1
Pembahasan:
Jawaban : A
2. Suatu gas ideal mula-mula menempati ruang yang volumenya V pada suhu T dan tekanan P. Jika suhu gas menjadi 3/2 T dan tekanannya menjadi 2 P, maka volume gas menjadi ….
A. 3/4 V
B. 4/3 V
C. 3/2 V
D. 3 V
E. 4 V
Pembahasan:
Jawaban : A
3. Sebanyak 3 liter gas Argon bersuhu 27°C pada tekanan 1 atm( 1 atm = 105 Pa) berada di dalam tabung. Jika konstanta gas umum R = 8,314 J mol−1 K−1 dan banyaknya partikel dalam 1 mol gas 6,02 x 1023 partikel, maka banyak partikel gas Argon dalam tabung tersebut adalah…..
A. 0,83 x 10²³ partikel
B. 0,72 x 10²³ partikel
C. 0,42 x 10²³ partikel
D. 0,22 x 10²³ partikel
E. 0,12 x 10²³ partikel
Pembahasan:
Jawaban : B
4. Tekanan gas dalam ruang tertutup:
- 1) Sebanding dengan kecepatan rata-rata partikel gas.
- 2) Sebanding dengan energi kinetik rata-rata partikel gas.
- 3) Berbanding terbalik dengan volume gas.
- 4) Tidak bergantung pada banyaknya partikel gas.
Pernyataan yang benar adalah…
A. 1, 2, dan 3
B. 1, 2, 3, dan 4
C. 1 dan 3
D. 2 dan 4
E. 4 saja
Pembahasan:
Lihat persamaan tekanan gas.
Jawaban: A
5. Dua mol gas menempati ruang 24,08 L. tiap molekul gas memiliki energi kinetik sebesar 3 . 10– 21 Joule. Jika bilangan Avogadro 6,02 . 1023 partikel maka tekanan gas dalam tangki adalah…
A. 1,00 . 10² Pa
B. 2,41 . 10² Pa
C. 6,02 . 10² Pa
D. 1,00 . 10^5 Pa
E. 2,41 . 10^5 Pa
Pembahasan:
Jawaban : D
Simak Juga : Soal Getaran Harmonik (Gerak Harmonis Sederhana)
6. Suatu gas ideal dengan tekanan P dan volume V. Jika tekanan gas dalam ruang tersebut menjadi ¼ kali semula pada volume tetap, maka perbandingan energi kinetik sebelum dan sesudah penurunan tekanan adalah…
A. 1 : 4
B. 1 : 2
C. 2 : 1
D. 4 : 1
E. 5 : 1
Pembahasan:
Jawaban : D
7. Sebuah ruang tertutup berisi gas ideal dengan suhu T dan kecepatan partikel gas di dalamnya v. Jika suhu gas itu dinaikkan 2T maka kecepatan partikel gas tersebut menjadi…
A. 2 v
B. ½ v
C. 2 v
D. 4 v
E. v2
Pembahasan:
Jawaban : A
8. Didalam sebuah ruang tertutup terdapat gas dengan suhu 27oC. Apabila gas dipanaskan sampai energi kinetiknya menjadi 5 kali semula, maka gas itu harus dipanaskan sampai suhu…
A. 100°C
B. 135°C
C. 1200°C
D. 1227°C
E. 1500°C
Pembahasan:
Jawaban : D
9. Sejumlah gas ideal dalam tabung tertutup dipanaskan secara isokhorik sehingga suhunya naik 4 kali semula. Energi kinetik rata-rata molekul gas ideal menjadi…
A. ¼ kali semula
B. ½ kali semula
C. Sama dengan semula
D. 2 kali semula
E. 4 kali semula
Pembahasan:
Dari persamaan energi kinetik gas Ek = 3/2 k T, menunjukkan energi kinetik sebanding dengan suhu. Artinya jika suhu naik 4 kali semula berarti energi kinetik naik 4 kali semula.
Jawaban : E
10. Suhu gas ideal dalam tabung dirumuskan mutlak dan Ek menyatakan energi kinetik rata-rata molekul gas. Berdasarkan persamaan tersebut…
A. Semakin tinggi suhu, energi kinetik semakin kecil.
B. Semakin tinggi suhu, gerak partikel semakin lambat.
C. Semakin tinggi suhu, gerak partikel semakin cepat.
D. Suhu gas berbanding terbalik dengan energi kinetik.
E. Suhu gas tidak mempengaruhi gerak partikel.
Pembahasan:
Dari persamaan energi kinetik gas Ek = 3/2 k T, menunjukkan energi kinetik sebanding dengan suhu. Sehingga semakin tinggi suhu maka energi kinetik makin besar. Energi kinetik makin besar maka gerak partikel makin cepat.
Jawaban : C
Sudah selesai membaca dan berlatih tentang soal ini ? Ayo lihat dulu Daftar Soal Fisika lainnya