Hukum Perbandingan Volume (Gaylussac) – Konsep, Bunyi dan Contoh Soal – Pada awalnya para ilmuwan menemukan bahwa gas hidrogen dapat bereaksi dengan gas oksigen membentuk air. Perbandingan volume gas hidrogen dan oksigen dalam reaksi tersebut tetap, yakni 2 : 1.

Kemudian di tahun 1808, ilmuwan Prancis, Joseph Louis Gay Lussac, berhasil melakukan percobaan tentang volume gas yang terlibat pada berbagai reaksi dengan menggunakan berbagai macam gas.
Data Percobaan Gay Lussac
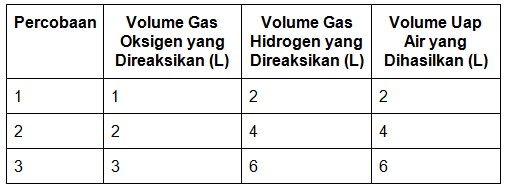
Pada penelitian itu ditemukan bahwa pada suhu dan tekanan tetap, setiap satu volume gas oksigen akan bereaksi dengan dua volume gas hidrogen menghasilkan dua volume uap air, dengan demikian perbandingan antara volume hidrogen, volume oksigen dan volume uap air berurut adalah 2 : 1 : 2.
Contoh lain : satu volume gas hidrogen akan bereaksi dengan satu volume gas klor menghasilkan dua volume gas hidrogen klorida; perbandingan volume hidrogen, volume klor dan volume hidrogen klorida berurut adalah 1 : 1 : 2. Pada reaksi antara gas nitrogen dan gas hidrogen membentuk gas amonik, maka perbandingan volume dari ketiga gas itu berturut adalah 1 : 3 : 2 (N2 : H2 : NH3).
Berdasarkan uraian di atas, dapat disimpulkan bahwa :
Bunyi Hukum Perbandingan Volume oleh Gay Lussac
“Pada suhu dan tekanan yang sama, perbandingan volume gas pereaksi dengan volume gas hasil reaksi merupakan bilangan bulat dan sederhana ( sama dengan perbandingan koefisien reaksinya )”.
Contoh :

Contoh Soal :
Sebanyak 8 L C₃H₈ dibakar habis dengan oksigen sesuai dengan persamaan reaksi
C₃H₈ + 5O₂ → 3CO₂ + 4H₂O
pada suhu dan tekanan yang sama volume gas CO2 yang dihasilkan adalah…
Penyelesaian :

Jadi, volume gas CO2 yang dihasilkan pada suhu dan tekanan yang sama adalah 24 L.
Baca Lebih Lengkap disini : 20+ Soal Hukum Dasar Kimia dan Jawaban [+Pembahasan]
Lihat Juga :



